
ზუსტ და საბუნებისმეტყველო მეცნიერებათა ფაკულტეტი
ინტერფაზური ბიონანომეცნიერება თბილისის სახელმწიფო უნივერსიტეტში: მიღწევები და პერსპექტივები საქართველოსთვის
ბიონანომეცნიერების და ბიონანოტექნოლოგიის კვლევის ობიექტების მრავალფეროვნება განუზომელია. ივ. ჯავახიშვილის სახელობის თბილისის სახელმწიფო უნივერსიტეტის ზუსტ და საბუნებისმეტყველო მეცნიერებათა ფაკულტეტის ბიოფიზიკისა და ბიონანომეცნიერების სამეცნიერო-კვლევითი ინსტიტუტის მონაწილეობით მიმდინარე საერთაშორისო კვლევებს საფუძველი 2000-2003 წლებში ჩაეყარა.
ნანომეცნიერების და მისი უმნიშვნელოვანესი კომპონენტის – ბიონანომეცნიერების, როგორც თანამედროვე ინტერდისციპლინური და მულტიდისციპლინური „ზედარგების”, აგრეთვე მათთან უშუალოდ და განუყოფლად დაკავშირებული გამოყენებითი მიმართულებების – ნანოტექნოლოგიის და ბიონანოტექნოლოგიის ისტორია სათავეს XX საუკუნის 60-იან წლებში იღებს. ტექნოლოგიურად განვითარებული, და ასევე, სწრაფად განვითარებადი ქვეყნების (აშშ, ევროგაერთიანება, იაპონია, ისრაელი, ჩინეთი, ინდოეთი და სხვა) სტრატეგიული განვითარების სახელმწიფო პროგრამებში, დაფინანსების თვალსაზრისით, მათ ერთ-ერთი ცენტრალური ადგილი დაიკავეს მეორე ათასწლეულის დასაწყისიდან. პრეფიქსი „ნანო“ (nano), ასევე აბრევიატურა „ნმ“ (nm), წარმოადგენს ტერმინ „ნანომეტრის“ (nanometer) შემოკლებულ ვარიანტს; ეს უკანასკნელი მიღებულია როგორც სიგრძის ერთეული და შეადგენს მეტრის ერთ მემილიარდედ ნაწილს (10-9 მ). განვითარების პირველ ეტაპზე, „ნანომატერიას“ ჩვეულებრივად უწოდებდნენ ნივთიერების ისეთ წარმონაქმნებს, რომელთა ზომა 100 ნმ-ზე ნაკლებია. თუმცა, როგორც შემდგომში აღმოჩნდა, ზოგიერთ შემთხვევაში გამყოფმა საზღვარმა შესაძლოა გაიაროს ბევრად უფრო „დაბლა“, 10, ან თუნდაც 1 ნმ-ის ნიშნულზე.
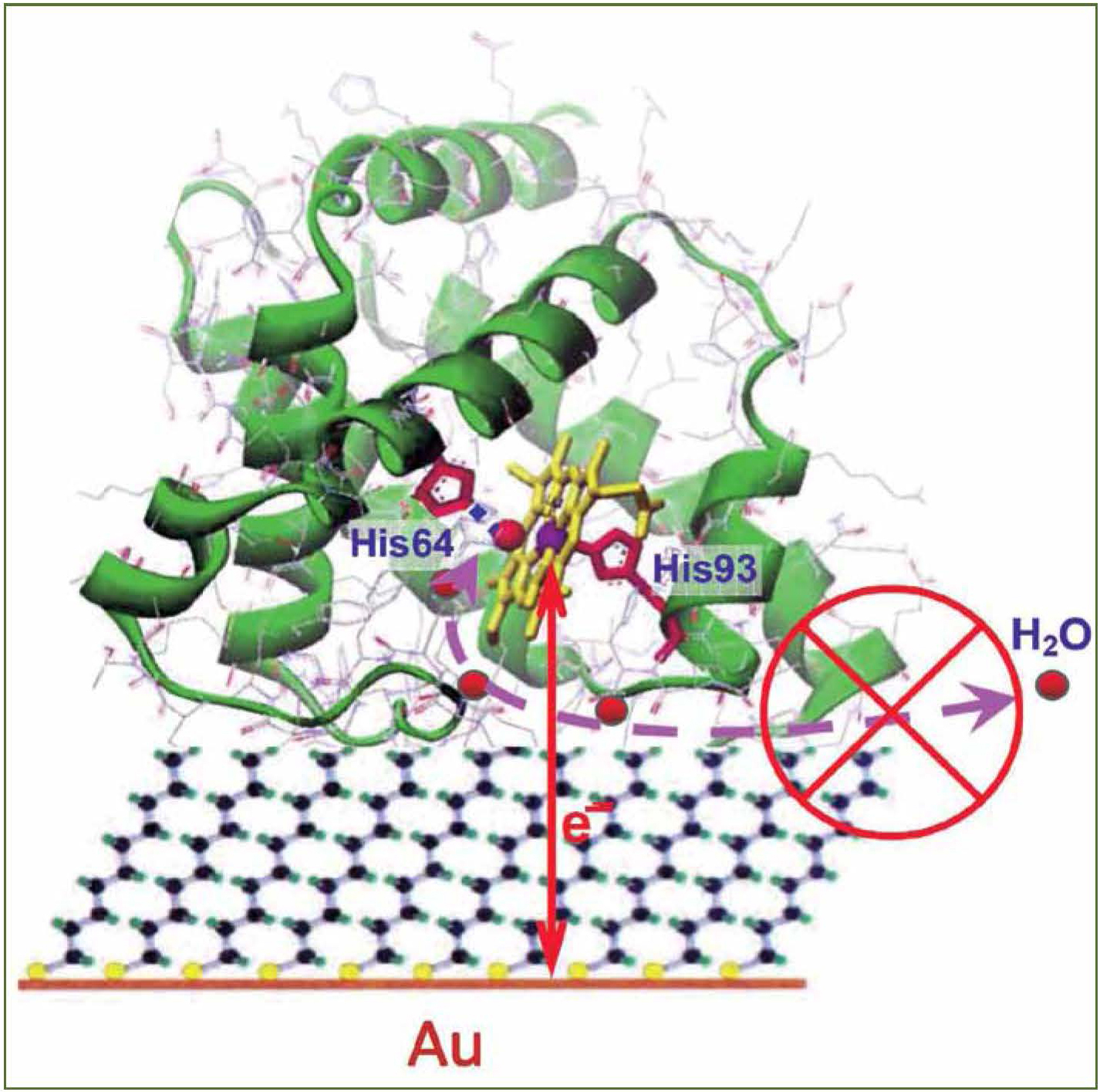
სურ. ჰიბრიდული ნანოსისტემის ერთ-ერთი ნიმუში, კარგად ცნობილი ცილის - მიოგლობინის (ზედა ნაწილი), თვითწყობადი ორგანული ფირის (შუა ნაწილი) და ოქროს მზიდი ელექტროდის (ქვედა ნაწილი) შემადგენლლობით.
წყარო: D.E.khoshtaria, et al. J. Phys. Chem. B., 2014, v.118, 692-706.
აღნიშნული „ზედარგების“ განსაკუთრებული, ინოვაციური სპეციფიკა სწორედ იმაში მდგომარეობს, რომ თუნდაც ერთგვაროვანი მატერიის (მაგალითად, ოქროსგან დამზადებული ბურთულის) რიგი ფიზიკური და/ან ქიმიური მახასიათებლები ამ „კრიტიკული მასშტაბის“ ორ სხვადასხვა მხარეს შეიძლება იყოს არსებითად განსხვავებული. აღსანიშნავია, რომ ბიოლოგიურად აქტიური მრავალი მაკრომოლეკულის, დნმ-ის, ცილების და ლიპიდების შემადგენელი, ხშირად ფუნქციის განმსაზღვრელი კომპონენტების ზომებიც ნმ-ის ან უფრო მცირე ზომებით ხასიათდება; ანუ ბიომოლეკულებიც, გარკვეული თვალსაზრისით, ნანონაწილაკებს ან ნანონაწილაკების ბუნებრივ აგრეგატებს წარმოადგენენ. მაგრამ, თანამედროვე ბიონანომეცნიერების და ბიონანოტექნოლოგიის ობიექტების ცნების ქვეშ, როგორც წესი, იგულისხმება ე.წ. „ჰიბრიდული“ ნანომეტრის მასშტაბის ზემოლეკულური აგრეგატები („სუპრამოლეკულური ანსამბლები“), რომლებშიც შესაძლებელია გაერთიანებული იყოს როგორც საკუთრივ ბიომოლეკულები და/ან მათი ფრაგმენტები, სინთეტური ქიმიური მოლეკულები (ხშირად, პოლიმერები), ასევე ნანომეტრის ზომის გამტარული (მეტალური) ან/და ნახევარგამტარული თვისებების მქონე მზიდი პლატფორმები (ელექტროდები) ან/და უმცირესი ნაწილაკები. სწორედ ასეთი პოტენციურად მულტიფუნქციური სუპერანსამბლების მრავალსახეობათა შექმნის პრაქტიკულად შეუზღუდავი შესაძლებლობები ქმნიან ბიონანოტექნოლოგიაში მათი გამოყენების უდიდეს პერსპექტივას.
ბიონანომეცნიერების და ბიონანოტექნოლოგიის კვლევის ობიექტების მრავალფეროვნება განუზომელია. ივ. ჯავახიშვილის სახელობის თბილისის სახელმწიფო უნივერსიტეტის ზუსტ და საბუნებისმეტყველო მეცნიერებათა ფაკულტეტის ბიოფიზიკისა და ბიონანომეცნიერების სამეცნიერო-კვლევითი ინსტიტუტის მონაწილეობით მიმდინარე საერთაშორისო კვლევებს საფუძველი ჩაეყარა 2000-2003 წლებში, ქ. ერლანგენის (გერმანია) და ქ. პიტსბურგის (პენსილვანია, აშშ) უნივერსიტეტებთან თსუ პროფესორის, ზუსტ და საბუნებისმეტყველო მეცნიერებათა ფაკულტეტის დოქტორის დიმიტრი ხოშტარიას მიერ ინტერფაზური ბიონანომეცნიერების მიმართულებით ინიცირებულ ერთობლივ სამეცნიერო პროექტების ფარგლებში, და დღესაც ხორციელდება გერმანული ა. ფონ ჰუმბოლდტის და ფოლკსვაგენის, აშშ ნაციონალური სამეცნირო საბჭოს (NRC) და ფულბრაიტის ფონდების ხელშეწყობით და დაფინანსებით. დაწყებული 2009 წლიდან, ანუ თსუ ბიოფიზიკისა და ბიონანომეცნიერების საფაკულტეტო სამეცნიერო-კვლევითი ინსტიტუტის დაარსების დღიდან თსუ მეცნიერთა ამ ჯგუფის პროექტები ასევე ფინანსდება შოთა რუსთაველის ეროვნული სამეცნიერო ფონდის მიერ (ივ. ბერიტაშვილის ბიომედიცინის ექსპერიმენტული ცენტრის ბიოფიზიკის განყოფილებასთან ერთად).
მეცნიერის განმარტებით, ინტერფაზური, ანუ ტიპურად, მყარ და თხევად ფაზათა გამყოფ პირობით საზღვარზე განთავსებული (გარკვეულწილად, ცოცხალ უჯრედში არსებულის მიბაძვით შექმნილი, – „ბიომიმეტიკური“) ბიონანოსისტემების მთავარი უპირატესობა მონოფაზურ სისტემებთან შედარებით ის გახლავთ, რომ ისინი იძლევიან მეტალურ მზიდ ფაზასა (პლატფორმას) და შესწავლის ბიოლოგიურ ობიექტს (აქტიურ ცენტრს) შორის ელექტრონების მიმოცვლის განხორციელების საშუალებას. აქ იგულისხმება, რომ ბიოლოგიური შესწავლის ობიექტის მთავარი ან მეორადი ბიოლოგიური ფუნქცია მოიცავს სწორედ „თავისუფალი“ ელექტრონის გადატანას ან ელექტრონის მონაწილეობას შედარებით უფრო კომპლექსურ პროცესში, მაგალითად, ყველასათვის ნაცნობი გლუკოზის მოლეკულის ფერმენტულ გარდაქმნაში. თავის მხრივ, ელექტრონების მიმოცვლა ან გადატანა იძლევა მკაფიო ვოლტამპერულ სიგნალს, რომლის სრულყოფილი ანალიზი შესაძლებელია ჩატარდეს დღეისთვის კარგად შემუშავებული ელექტროქიმიური მეთოდოლოგიის – სწრაფი სკანირების (1000 ვოლტამდე წამში) ციკლური ვოლტამეტრიის გამოყენებით. რაც მთავარია, ამ ტიპის სისტემებში ცვალებადი სისქის თხელი ორგანული არაგამტარი ფირების, როგორც ცილასა და მეტალის ელექტროდს შორის გამყოფი ფენის ფაქტობრივად ერთი ატომის სიზუტით ვარირების შესაძლებლობას იძლევა, რათა თანდათან, წარმოუდგენლად დიდი სიზუსტით ვცვალოთ მუხტის (ელექ-ტრონის) გადატანის მანძილი დაახლოებით ერთი ანგსტრემის, ანუ 0.1 ნმ (ნახშირბადის ატომის ზომის) ნაბიჯებით. თანდართულ სურათზე საილუსტრაციოდ წარმოდგენილია სწორედ თსუ მეცნიერთა ჯგუფის მიერ ახლახან საფუძვლიანად შესწავლილი ჰიბრიდული ნანოსისტემის ერთ-ერთი ნიმუში, კარგად ცნობილი ცილის – მიოგლობინის (ზედა ნაწილი), თვითაწყობადი ორგანული ფირის (შუა ნაწილი) და ოქროს მზიდი ელექტროდის (ქვედა ნაწილი) შემადგენლობით. სურათზე კარგად იკვეთება ცილის ე.წ. ჰემის ჯგუფი (ყვითელი ფერით), რკინის იონით ცენტრში (შინდისფერი ბურთულა) და მოძრავი წყლის მოლეკულის სხვადასხვა პოზიცია და სავარაუდო ტრაექტორია (შესაბამისად წითელი ბურთულები და ვარდისფერი წყვეტილი ისარი). ვერტიკალური ორმხრივი წითელი ისარი ასახავს ელექტრონის მიმოცვლის უმოკლეს გზას.
ერთობლივ სამეცნიერო პროექტების ფარგლებში, ძირითადად ზემოაღიშნული მეთოდოლოგიის გამოყენებით (უფრო თანამედროვე დასახელებით: „Protein Film Voltammetry“) პროფესორ დიმიტრი ხოშტარიას ხელმძღვანელობით შესწავლილი იყო რიგი ჟანგვა-აღდგენითი უნარის მქონე („რედოქსაქტიური“) ცილებისა, მათ შორის: ციტოქრომ c-ს (Cyt-c), აზურინის (Az) და მიოგლობინის (Mb) მონაწილეობით მიმდინარე მუხტის გადატანის, ანუ ცვალებადი სისქის თხელი ორგანული ფირებით მოდიფიცირებულ ელექტროდებთან ელექტრონების მიმოცვლის „ელემენტარული“ (შინაგანი) მექანიზმები. სისტემატური კვლევების შედეგად, რიგი ფიზიკო-ქიმიური მიდგომების (გარემოს ტემპერატურის, ჰიდროსტატიკური წნევის, სიბლანტის, ქიმიური შემადგენლობის ცვალებადობის და სხვა) კომბინირებული გამოყენების საშუალებით, პირველად იქნა საიმედოდ დადგენილი, რომ ბიომოლეკული ელექტრონის გადასვლების ფიზიკური ბუნება შესაძლებელია შეიცვალოს (გარდაისახოს) ორ ზღვრულ რეჟიმს შორის მუხტის გადატანის მანძილის 1-2 ანგსტრემის ფარგლებში ცვლილებისას. ამ დასკვნას უდიდესი მნიშვნელობა ენიჭება ინტერფაზური ბიონანომეცნიერების როგორც ფუნდამენტური, ისე გამოყენებითი (ბიონანოტექნოლოგიური) რიგი მიმართულებების შემდგომი განვითარებისთვის.
ყოველივე ზემოაღნიშნული მიუთითებს იმაზე, რომ საქართველოში, კერძოდ თსუ-ში, არსებობს ინტერფაზური ბიონანომეცნიერების მიმართულებით თანამედროვე საერთაშორისო დონის მოწინავე ხაზზე მომუშავე ინტერდისციპლინური სამეცნიერო სკოლა. შესაბამისად – მასზე დამყარებული ინტერფაზური ბიონანოტექნოლოგიების აღმოცენების და ფართო განვითარების საკმარისად კარგი პერსპექტივა. მაგრამ ამისთვის, დიმიტრი ხოშტარიას აზრით, საჭიროა ისე, როგორც ეს მოხდა მსოფლიოს ეკონომიკურად განვითარებულ და მდგრადად განვითარებად ქვეყნებში – ამ მიმართულებების საქართველოსთვის პრიორიტეტულ მიმართულებებად აღიარება და შესაბამისი სახელმწიფო პოლიტიკის გატარება.
რატომ არის ეს მსოფლიოსთვის და საქართველოსთვის დღეს ესოდენ აქტუალური? მეცნიერის პასუხი შემდეგია:
(ა) მსოფლიოს მოწინავე ქვეყნებში წამყვანი მეცნიერების მიერ გაკეთებული სტრატეგიული პროგნოზების თანახმად, მომავლის ნანოტექნოლოგიების უდიდესი ნაწილი, მათ შორის, მზის ენერგიის გამოყენების, ბიოსაწვავის გადამუშავების, ბიოსენსორული და იმუნოსენსორული მიმართულებები, დაემყარება ფაზათაშორის, მუხტის (ელექტრონის და/ან პროტონის) გადატანის კვანტურ-მექანიკურ თავისებურებათა ადექვატურად ამსახველ ბიონანომეცნიერებას.
(ბ) ინტერფაზური ბიონანომეცნიერების და ბიონანოტექნოლოგიის მიმართულებებით კვლევები მეტად იაფია, ძირითადად ემყარება საერთაშორისო და ადგილობრივ ინტელექტუალურ, და არა ქვეყნის ინდუსტრიულ, პოტენცალს. ამდენად, მინიმალური ხელშეწყობის პირობებშიც კი შესაძლებელია განვითარდეს სწრაფად ან თუნდაც ნახტომისებურად.
(გ) ამდენად, საკუთრივ ინტერფაზური ბიონანომეცნიერების და ბიონანოტექნოლოგიის მიმართულებების განვითარება შეიძლება გახდეს ერთ-ერთი უპირველესი (შესაძლოა უმთავრესი) წინაპირობა საქართველოს სწრაფი ეკონომიკური განვითარებისთვის და მისი ევროპულ თუ მსოფლიოს სხვა მოწინავე ქვეყნებთან ეკონომიკური ინტეგრაციისთვის.
თსუ მეცნიერთა მონაწილეობით ამ მიმართლებით განხორციელებული კვლევების შესახებ მასალები გამოქვეყნებულია არაერთ ცნობილ სამეცნიერ ჟურნალში, მათ შორის აღსანიშნავია: D.E. Khoshtariya, T.D. Dolidze, M. Shushanyan, & R. van Eldik, Long-range electron transfer with myoglobin immobilized at Au/mixed-SAM junctions: Mechanistic impact of the strong protein confinement. J. Phys. Chem. B., 2014, v.118, 692-706.; D.H. Waldeck & D.E. Khoshtariya, Fundamental studies of long- and short-range electron exchange mechanisms between electrodes and protein In: Modern aspects of Electrochemistry. Applications of Electrochemistry and Nanotechnology in Biology and Medicine V.52, (N. Elias, Ed.) Springer Publishers, 2011, Chapter 2, p.105-238.; D.E. Khoshtariya, T.D. Dolidze, M. Shushanyan, K.L. Davis, D.H. Waldeck & R. van Eldik, Fundamental signatures of short- and long-range electron transfer for azurin functionalized at Au/alkanethiol SAM junctions, Proc. Natl. Acad. Sci. USA, 2010, v.107, p.2757-2762.; D.E. Khoshtariya, J. Wei, H. Liu, H. Yue, & D. H. Waldeck, The charge-transfer mechanism for cytochrome c adsorbed on nanometer thick films. Distinguishing frictional control from conformational gating. J. Am. Chem. Soc., 2003, v.125, p.7704-7714.




